儿茶素生物纳米材料抗炎和
抗氧化活性研究进展
活性氧(ROS)是机体代谢过程中产生的重要中间产物,当ROS过度表达不能被及时清除时,过量的ROS可能和脂质、蛋白质、多糖以及核酸等具有生物活性的大分子相互作用,引发细胞代谢紊乱、细胞器功能异常,导致许多疾病的发生,包括炎症、癌症、心血管疾病和神经退行性疾病,以及衰老[28-30]。
利用外源性抗氧化物质缓解氧化应激是治疗氧化应激损伤的一个重要策略。EGCG作为天然的抗氧化剂,由于其特殊的分子结构,可以和体内过量自由基反应,表现出很强的抗氧化性。
Sekowski等[31]研究表明,在UVB辐射前添加浓度为1~20 µmol·L-1的EGCG可以通过防止脂质过氧化、还原型谷胱甘肽和血红蛋白氧化来保护红细胞免受紫外线诱导的氧化损伤,结果表明EGCG能抑制UVB诱导的红细胞氧化应激。
Zhang等[32]将EGCG与Cu2+和PLLA自组装负载雷帕霉素实现了对血管愈合和炎症的调控。
Yang等[33]提出了一种新型的绿色纳米颗粒制备策略,以EGCG为原料,通过绿色酶聚合化学方法制备绿色纳米颗粒。该绿色纳米颗粒可以可以有效预防细胞内氧化损伤,加速伤口恢复,并保护肾脏免受急性肾损伤模型中活性氧的损害。
Hu等[34]将淀粉样蛋白和EGCG进行自组装成具有调节肠道微生物和抗炎作用的生物材料可显著改善由DSS诱导的小鼠结肠炎,促进肠道屏障功能,抑制促炎mRNA表达,具有广阔的胃肠道抗炎应用前景。
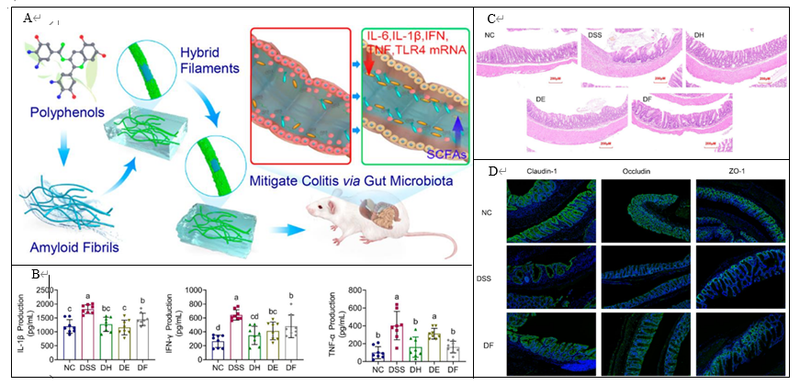
△ 图4 多酚纳米材料合成和体内试验
4
儿茶素药物递送系统研究进展
药物在病灶部位的精准释放是药物递送需要解决的一大难题。研究者们通常对药物进行抗体、靶向小肽或pH敏感分子修饰来提高药物在病灶部位的富集程度,从而实现高效低毒的治疗目标。
但值得一提的是这些修饰过程不仅复杂,而且还会引入新的分子,影响药物代谢,甚至会产生严重的毒副作用。
因此,一种简单有效的药物递送系统的建立是亟需解决的难题。
EGCG凭借其多酚羟基的结构特殊性和天然的生物活性,有望成为新型药物递送系统的备选物质,不仅能实现药物递送,还能起到协同作用。
Shen等[35]开发了一种具有高效siRNA传递效率的核壳结构纳米颗粒,该纳米球可以将siRNA高效的递送到细胞内部,使其能够选择性调控靶基因,有效治疗DSS诱导的结肠炎。
Fan等[36]利用不同的直接聚合方法设计和合成了儿茶酚胺聚合物,用于siRNA在体外和体内的传递,从而大大提高其复合物的生物稳定性、细胞递送和基因沉默效率。
上述结果表明,儿茶素有望被开发为一种简单通用的药物递送系统,用于疾病治疗。
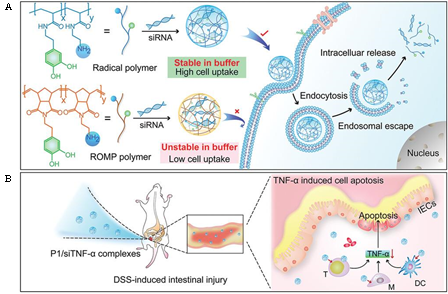
△ 图5 聚合物构建和靶向递送示意图
5
儿茶素生物纳米材料抗病毒
研究进展
近年来禽流感、H7N9、新型冠状病毒等疫情的发生,严重危害了畜禽和人类的生命安全,阻碍了社会进一步发展。
在这过程中,一些相关的研究学者们发现EGCG对一些病毒有高效抑制作用[37-42]。
Ge等[43]研究EGCG抗猪繁殖与呼吸综合征病毒(PRRSV),发现EGCG均能有效抑制PRRSV复制,且有剂量依赖性,在浓度为125 µmol·L-1时,可以完全抑制病毒的感染。
Williamson等[44]研究发现,EGCG可以通过抑制HIV-1糖蛋白(gp)120与T细胞上CD4分子的结合,从而降低HIV-1的传染性。
Calland等[45]证明了EGCG可以直接通过结合病毒颗粒和干预脂质代谢的方式来预防HCV感染细胞。
也有相关研究认为EGCG是植物化学物质中最具有潜力的3CLpro抑制,可用于COVID-19的预防治疗。
对此,Zhang等[46]综述了EGCG的潜在抗新冠病毒机制,EGCG可以通过直接抗氧化、激活Nrf2通路、调控炎症风暴等来抑制氧化应激和下调血管紧张素转换酶2(ACE2)的表达,从而抑制病毒的感染和复制。
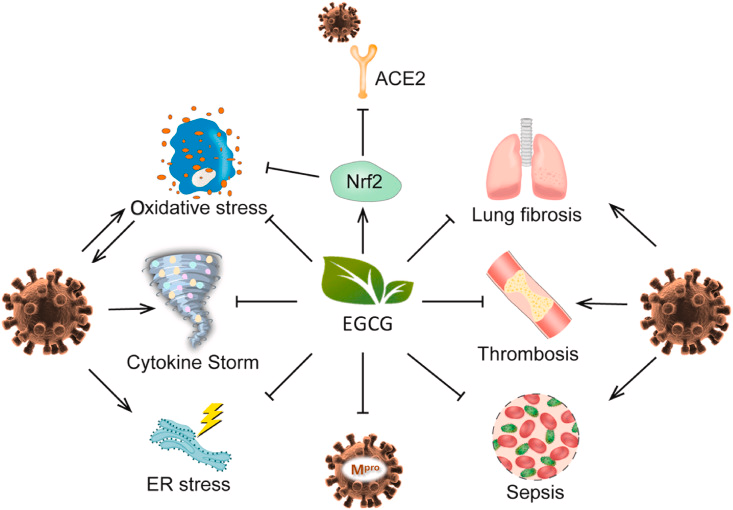
△ 图6 EGCG抗新冠病毒的潜在分子机制
6
小结
借助纳米生物技术将儿茶素与金属、天然高分子、脂质体、壳聚糖等构建新型生物医用纳米材料,不仅提高了儿茶素的生物利用度,还能使其负载临床小分子药物达到协同作用。
这种以儿茶素作为配体构建新型生物材料的策略拓展了儿茶素在新型生物医用材料构建中的应用,有望推动茶资源,特别是多酚含量高的夏秋茶资源的高效利用。
但同时也存在诸多问题——
一是生物安全问题。虽然通过功能配体的修饰可以有效提升儿茶素在生物体内的利用度,但是,由于这些生物材料复杂的设计工艺,使其在体内降解困难。
二是结构复杂的生物纳米材料容易在血液循环过程中形成蛋白冠而失去功能,难以抵达病灶深层部位[47-49];再加上复杂的结构设计很难解析儿茶素纳米药物在体内代谢规律以及发挥生物功能的分子机制。
因此,针对特定的疾病模型,设计结构简单、生物安全和功能明确的个性化儿茶素生物材料是推进其应用的基础。
此外,天然药物在病灶部位的靶向递送一直是近几年材料化学和生物医学研究的热点和难点[50-52]。将儿茶素精准递送到病灶部位,或者以儿茶素为递送系统将临床药物递送到病灶部位是提高药物疗效和降低毒副作用的有效手段[53]。
总之,在保证儿茶素生物材料充分发挥活性的前提下,低成本实现规模化制备是推动儿茶素生物材料临床前大规模动物评价的关键。
来源:中国茶叶学会
若有侵权请联系删除













暂无评论